









 Rada pro výzkum, vývoj a inovace: Seznam recenzovaných neimpaktovaných časopisů vydávaných v ČR
Oficielní časopis České společnosti pro ultrazvuk v porodnictví a gynekologii.
Rada pro výzkum, vývoj a inovace: Seznam recenzovaných neimpaktovaných časopisů vydávaných v ČR
Oficielní časopis České společnosti pro ultrazvuk v porodnictví a gynekologii.

Preeklampsia (PE) je jedna z najčastejších a najnebezpečnejších komplikácii tehotenstva. Vysoká mortalita a morbidita matky a plodu poukazujú na potrebu jej včasnej predikcie a prevencie. Množstvo rozsiahlych štúdii sa zameriava na včasný skríning preeklampsie, zamedzenie jej vzniku a úspešnú liečbu. Autorka článku počas dvojročnej praxe v Nadácií fetálnej medicíny v Londýne (The Fetal Medicine Foundation, FMF) pod vedením profesora Nicolaidesa sa podieľala na štúdiách SPREE, ASPRE a EVENTS, ktoré viedli k vytvoreniu nového manažmentu preeklampsie. Cieľom článku je predstaviť vývoj a výhody kombinovaného skríningu v 11. – 13.+6 gestačnom týždni na výpočet rizika preeklampsie. Doposiaľ hlavným výstupom prvotrimestrálneho skríningu boli riziká aneuploidií, ale v súčasnosti sa výpočet rizík rozšíril aj na tehotenské komplikácie ako sú preeklampsia, intrauterinná rastová reštrikcia a predčasný pôrod. Štúdia ASPRE ukázala efektivitu v preventívnom podávaní aspirínu 150 mg vo večerných hodinách pacientkam s vysokým rizikom PE od 12. do 36. týždňa gravidity. Tento rok FMF tím navrhol nové skríningové stratégie, ktoré závisia od toho, ktorý biomarker sa využíva (PAPP-A vs. PlGF). Najefektívnejší skríning preeklampsie je s využitím PlGF. Keďže sa rutinne v prvom trimestri odoberá PAPP-A pre skríning aneuploidií, z tohto dôvodu bolo v štúdiách sledované a potvrdené aj jeho využitie v rôznych kombináciách skríningových stratégií v snahe dosiahnuť porovnateľnú senzitivitu ako pri skríningu s PlGF. Ďalším nedávnym úspechom bolo vypracovanie prvotrimestrálneho kombinovaného skríningu preeklampsie u dvojčiat.
Preeklampsia (PE) je multisystémové ochorenie, ktoré sa rozvíja počas druhej polovice tehotenstva. Odporúčanie ISSHP (International Society for the Study of Hypertension in Pregnancy) z roku 2018 definuje PE ako de novo vzniknutú hypertenziu po 20. gestačnom týždni a proteinúriu a/alebo maternálnu orgánovú dysfunkciu a/alebo uteroplacentárnu dysfunkciu. Maternálna orgánová dysfunkcia je definovaná novým vznikom nasledujúcich komplikácií: renálna insuficiencia, hepatálna dysfunkcia, neurologické a hematologické komplikácie (1).
V súčasnej klinickej praxi sa za zásadné považuje delenie PE podľa doby nástupu ochorenia. Výskyt PE pred 34. gestačným týždňom sa hodnotí ako včasná PE. Je spojená s vyššou morbiditou matky a asi 4-krát vyšším rizikom intrauterinného úmrtia plodu. PE po 34. gestačnom týždni sa označuje ako neskorá (2). Ďalej sa PE rozdeľuje na pretermínovú, teda pred 37. týždňom tehotenstva, ktorá postihuje jednu tretinu tehotných s PE a termínovú PE, po 37. týždni tehotenstva, ktorá postihuje dve tretiny tehotných s PE (3).
PE sa vyskytuje u 2 – 5 % tehotenstiev. Miera výskytu závisí od demografických charakteristík vyšetrovanej populácie (3). Odhadovaná incidencia PE u dvojičiek je 9 %, čo je 3-násobne viac ako pri jednoplodových tehotenstvách. Treba brať do úvahy aj fakt, že pôrod dvojičiek je spravidla v skoršom gestačnom veku v porovnaní s jednoplodovým tehotenstvom. Francisco a kol. porovnali celkový výskyt PE a incidenciu pretermínovej PE medzi dvojičkami a jednoplodovými tehotenstvami. Vo výsledkoch ich štúdie sa poukazuje na podhodnotenie rizika pretermínovej PE u gemín, ktoré je 9-krát vyššie ako u jednoplodových tehotenstiev (4).
Tradičný prístup ako identifikovať ženy s vysokým rizikom PE je založený na anamnéze a vyhodnotení viacerých rizikových faktorov. Odporúčanie NICE (National Institute for Health and Clinical Excellence) vo Veľkej Británii a odporúčania ACOG (American College of Obstetricians and Gynecologists) v USA využívajú tradičný prístup. Ide o jednoduché predikcie rizika PE, ktoré sú založené len na tzv. skórovacom systéme.
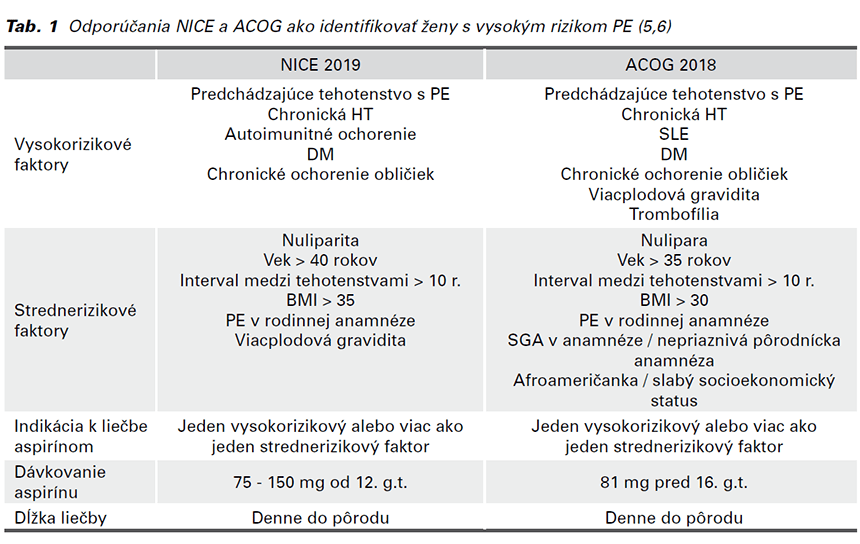
V tabuľke 1 sú uvedené obe odporúčania. Odporúčanie NICE zaraďuje ku vysokorizikovým faktorom predchádzajúce tehotenstvo s PE, chronické ochorenie obličiek, chronickú hypertenziu (HT), diabetes mellitus (DM) a autoimunitné ochorenia ako systémový lupus erythematosus (SLE) alebo antifosfolipidový syndróm (APS). Ak pacientka má jeden z vysokorizikových faktorov alebo aspoň jeden zo strednerizikových faktorov, jej gravidita je považovaná za rizikovú. Pacientka má denne užívať 75 - 150 mg aspirínu od 12. týždňa gravidity až do pôrodu (5). Odporúčanie ACOG zahŕňa širší okruh rizikových faktorov. Ak pacientka má jeden z vysokorizikových faktorov alebo aspoň jeden zo strednerizikových faktorov, ACOG odporúča začať s dennou liečbou 81 mg aspirínu medzi 12. až 28. gestačným týždňom (optimálne pred 16. gestačným týždňom) až do pôrodu (6).
V roku 2017 O’Gorman a kol. porovnali senzitivitu skríningu PE podľa odporúčania NICE a odporúčania ACOG. Zistili, že NICE identifikuje okolo 40 % prípadov pretermínovej PE pri 10 % falošnej pozitivite (FP). Odporúčanie ACOG označuje dve tretiny populácie ako skríning–pozitívne. Senzitivita odporúčania ACOG je vysoká, okolo 90 %, ale pri 64 % FP (7). Výsledky tejto štúdie poukazujú na nevýhody odporúčaní: skórovací systém NICE má nízku senzitivitu a skórovací systém ACOG má veľmi vysoké percento FP.
FMF pod vedením prof. Nicolaidesa sa posledné desaťročie venuje vypracovaniu presnejších a “na mieru šitých” odporúčaní pre skríning PE. Počas dvojročnej praxe u prof. Nicolaidesa som mala možnosť sa podieľať na štúdiách SPREE (Screening ProgRamme for prE-Eclampsia) a ASPRE (ASpirin for evidence -based PREeclampsia prevention), ktoré viedli k vytvoreniu nového manažmentu PE jednoplodových tehotenstiev. Vypracovanie modelu na výpočet rizika PE využíva Bayesov princíp a štatistickú metódu logistickej regresie. Skríning kombinuje apriórne riziko (ktoré vychádza z maternálnych rizikových faktorov a jej anamnézy) a výsledky rôznych kombinácií biofyzikálnych a biochemických meraní. Metóda je založená na teórii, že ak by tehotenstvo nebolo ohraničené termínom pôrodu v 40. týždni, došlo by k rozvoju PE u všetkých žien. Na základe vyššie uvedenej kombinácie (apriórne riziko + biomarkery) sa pacientke stanoví vlastná Gaussova krivka distribúcie gestačného veku, podľa ktorej by mala vzniknúť PE. Takým-
to spôsobom je možné každej pacientke špecifikovať individualizované riziká rozvoja jednotlivých typov PE (včasná vs. neskorá, pretermínová vs. termínová). Rozvoj PE závisí od časového vzťahu medzi reálnym termínom pôrodu a individualizovane stanovenou Gaussovou krivkou. Pri nízkorizikových tehotenstvách je krivka posunutá doprava (Obr. 1), čoho dôsledkom je, že dôjde k pôrodu pred vznikom PE. Pri vysokorizikových tehotenstvách je posun doľava. Čím nižší je gestačný vek, v ktorom sa má rozvinúť PE, tým väčšie je riziko PE (8).
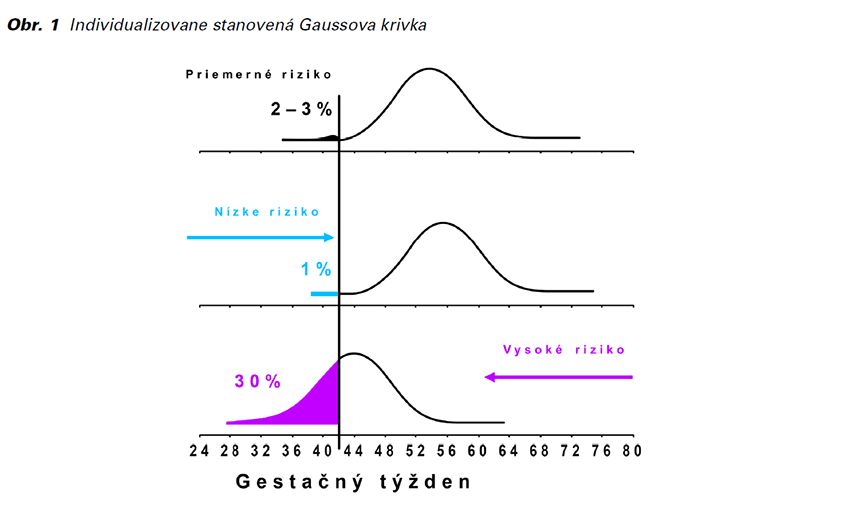
Výpočet rizika PE: rozvoj PE závisí od časového vzťahu medzi reálnym termínom pôrodu a individualizovane stanovenou Gaussovou krivkou. Pri nízkorizikových tehotenstvách je krivka posunutá doprava, čoho dôsledkom je, že dôjde k pôrodu pred vznikom PE. Pri vysokorizikových tehotenstvách je posun doľava. Čím nižší je gestačný vek, v ktorom sa má rozvinúť PE, tým väčšie je riziko PE (8).
Maternálne faktory (MF), ktoré zvyšujú riziko PE, sú: vyšší vek matky, nadváha, afro-karibský alebo juhoázijsky pôvod, HT, DM, SLE alebo APS, in vitro fertilizácia a PE v rodinnej alebo osobnej anamnéze (9).
Model využíva vo výpočte okrem MF aj hodnotenie biomarkerov, ktoré sú vyjadrené v násobkoch mediánu (multiples of median, MoM). Medzi biofyzikálne markery patrí stredný arteriálny tlak (mean arterial pressure, MAP) a meranie indexu pulzatility uterinných artérií (UTPI). Medzi biochemické markery, ktoré sa v štúdiách sledovali, boli zaradené tehotenský proteín A asociovaný s plazmou (PAPP-A), sérový placentárny rastový faktor (PlGF), antiangiogénny faktor sFLT-1 a fetálna DNA izolovaná z periférnej krvi tehotnej. V ďalších analýzach sa neukázali fetálna DNA a sFLT-1 výhodné pre začlenenie do kombinovaného skríningu (10,11,12,13).
Výhodou takého “na mieru šitého” rizika PE je, že ide o prísne individualizovaný prístup. Na rozdiel od iných skríningových stratégii berie sa do úvahy, že PE môže vzniknúť v ktoromkoľvek gestačnom veku, využíva maternálne rizikové faktory a súčasne aj hodnoty biomarkerov.
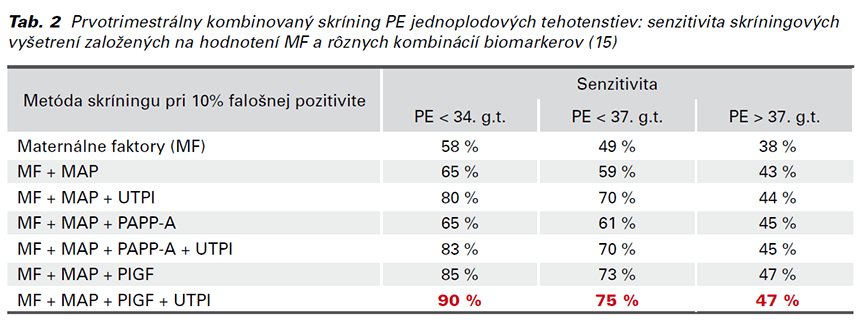
V roku 2017 prof. Nicolaides predstavil v prospektívnej validačnej štúdii koncept kombinovaného skríningu PE v 11. – 13.+6 gestačnom týždni s názvom SPREE. Táto multicentrická kohortná štúdia hodnotila pri každej randomizovanej pacientke MF a hodnoty biomarkerov (MAP, UTPI, PAPP-A a PlGF). Z výsledkov štúdie SPREE vyplýva, že najefektívnejšia kombinácia pre skríning PE je: MF + MAP + UTPI + PlGF (Tab. 2). Takýto skríning identifikuje približne 90 % včasnej formy PE, 75 % pretermínovej PE a 45 % termínovej PE pri 10 % FP (14,15).
Stratégiu manažmentu FMF tím zvolil tak, že skríning sa vykonáva na celej populácii pacientok (Obr. 2). Do vysokorizikovej skupiny sú zaradené tie, ktoré majú riziko ≥ 1:100 rozvoja pretermínovej PE. Ide približne o 10 % tehotných z celej populácie. Až u 75 % z nich dôjde k rozvoju PE. Práve táto skupina žien môže profitovať z liečby kyselinou acetylsaliciovou (ASA). Preventívna terapia ASA 150 mg vo večerných hodinách od 12. do 36. týždňa zníži riziko pretermínovej PE o 62 %. Do nízkorizikovej skupiny sú zaradené pacientky, ktoré majú riziko < 1:100. Túto skupinu tvorí 90 % vyšetrovanej populácie. Vznik pretermínovej PE je tu nepravdepodobný, ale je nutné prehodnotiť riziko ešte v 20. gestačnom týždni (16).

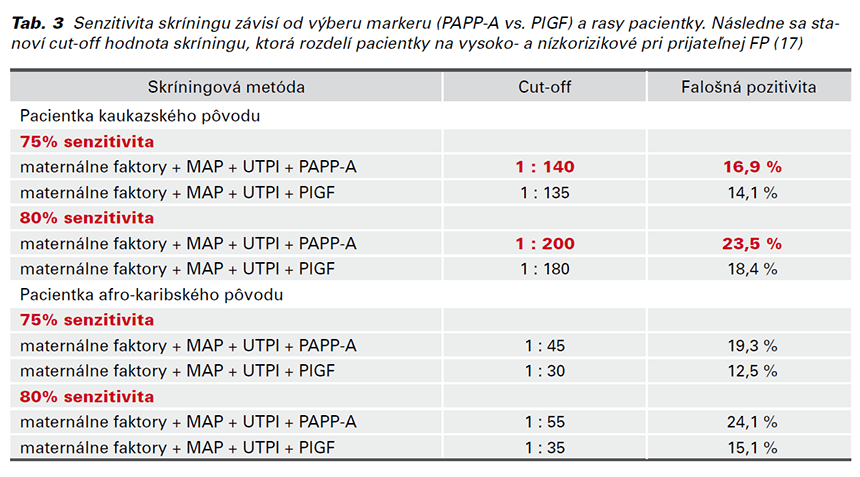
Vyššie uvedené skríningové stratégie uprednostňujú hodnotenie biomarkeru PlGF. V praxi sa rutinne a globálne v prvom trimestri odoberá PAPP-A pre skríning aneuploidií. Z tohto dôvodu je jeho využitie pri skríningu PE efektívnejšie a hlavne ekonomickejšie. Danej problematike a možnosti uplatnenia PAPP-A v prvotrimestrálnom kombinovanom skríningu PE sa venovali Mazer Zumaeta a kol. Síce vo svojej štúdii potvrdili nadradenosť skríningu využívajúceho PlGF, ale ponúkli aj možnosť klinického využitia PAPP-A pri prijateľnej FP. Pre porovnanie, senzitivita kombinovaného skríningu s PlGF (MF + MAP + UTPI + PlGF) je o 7,1 % vyššia ako s PAPP-A (MF + MAP + UTPI + PAPP-A) pri rovnakej FP (10 %). Senzitivita skríningu závisí od výberu markeru (PAPP-A vs. PlGF) a rasy pacientky. Následne sa stanoví cut-off hodnota skríningu, ktorá rozdelí pacientky na vysoko- a nízkorizikové. V Tab. 3 sú porovnania rôznych kombinácií skríningových stratégií. Ako príklady sú v článku ďalej uvedené skríningové stratégie u pacientok kaukazskej rasy, ktoré dominujú v našej populácii: ak je cieľom dosiahnuť 75 % senzitivitu, cut-off hodnotu si stanovíme 1:136 pri skríningu s PlGF pri FP 14,1 %, a 1:140 pri skríningu s PAPP-A pri FP 16,9 %. Ak je cieľom dosiahnuť 80 % senzitivitu, cut-off hodnotu si stanovíme 1:180 pri skríningu s PlGF pri FP 23,5 %, a 1:200 pri skríningu s PAPP-A pri FP 18,4 % (17). Štúdia ponúka možnosť zakomponovať PAPP-A do kombinovaného skríningu, ale treba si uvedomiť nárast FP podľa požadovanej senzitivity.
Štúdie FMF udávajú, že výskyt PE sa nezníži pokojom na lôžku, obmedzením fyzického pohybu alebo diétou, vrátane obmedzenia príjmu soli alebo doplnkov stravy s magnéziom, zinkom, kyselinou listovou, vitamínom C, D a E alebo rybacieho oleja (18).
Najúspešnejšia štúdia o účinnosti ASA pri prevencii PE bola ASPRE z roku 2017. Táto multicentrická, prospektívna, dvojito zaslepená štúdia analyzovala kombinovaný multimarkerový skríning a liečbu ASA ako prevenciu PE. Skríning PE sa vykonával v 11. – 13.+6 gestačnom týždni podľa FMF algoritmu u približne 27 000 jednoplodových gravidít (Obr. 3). Vysokorizikovým pacientkam bol náhodne pridelený buď aspirín v dávke 150 mg/deň alebo placebo. Liečba aspirínom viedla ku 62 % poklesu výskytu pretermínovej PE a 82 % redukcii včasnej PE (19).
Sekundárna analýza údajov zo štúdie ASPRE poukázala na to, že priaznivé účinky aspirínu závisia od compliance pacientky. Pokles výskytu pretermínovej PE môže byť približne o 75 % pri tých, ktorých compliance je ≥ 90 % a o 40 % pri tých, ktorých compliance je < 90 %. Z tohto dôvodu je veľmi dôležité pri zahájení liečby pacientku informovať, že dodržiavanie terapie môže priaznivo ovplyvniť prevenciu PE. Ak sa ASA neužíva každý deň, prevencia je nedostatočná a hrozí, že sa nepredíde vzniku ochorenia. Navyše sekundárna analýza poukázala na to, že v prevencii PE pri chronickej HT aspirín nemusí byť užitočný (20). I keď v súčasnosti nie sú dostupné dôkazy o priaznivých účinkoch ASA pri chronickej HT, napriek tomu jeho užívanie sa vysokorizikovým pacientkam odporúča.
Pri vytváraní skríningového modelu u gemín FMF tím využil dva súbory pacientok. Prvý súbor pochádzal z medzinárodnej štúdie EVENTS (Early vaginal progesterone for the preVention of spontaneous prEterm birth iN TwinS), ktorá prebehla od 2017 do 2019 a zahŕňala 1 798 pacientok. Druhý súbor viacplodových tehotenstiev pochádzal z prospektívnej štúdie o skríningu tehotenských komplikácií od 2006 do 2015 a zahŕňal 3 938 pacientok.
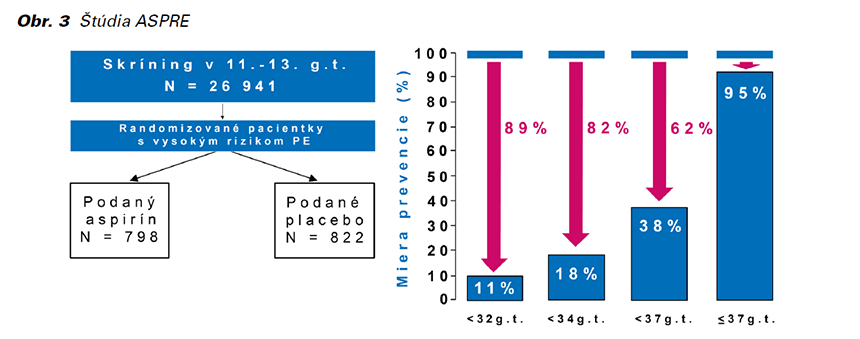
Liečba aspirínom viedla ku 62 % poklesu výskytu pretermínovej PE, ku 82 % poklesu výskytu včasnej PE a 89 % poklesu výskytu PE pred 32. gestačným týždňom (18).
FMF tím využil rovnaký apriórny model ako pri jednoplodových tehotenstvách. Apriórne riziko vychádzalo z MF a anamnézy. Biomarkery boli vyjadrené v MoM. Použitím Bayesovho princípu a modelu hodnotenia kompetitívnych rizík sa stanovila pacientke vlastná Gaussova krivka distribúcie gestačného veku, v ktorom dôjde k rozvoju PE. Ďalej bol navrhnutý model, pri ktorom efekt gemín posunie krivku doľava. Tento posun závisel od apriórnej strednej hodnoty. Posun doľava bol väčší, ak apriórna stredná hodnota bola vyššia. Posun doľava bol menší, ak apriórna stredná hodnota bola menšia.
Najlepšie výsledky skríningu boli potvrdené pri kombinácii MF, MAP, UTPI a PlGF (Tab. 4). Senzitivita skríningu je lepšia pri výpočte rizika PE pred 32. ako pred 37. gestačným týždňom. Začlenenie PAPP-A do skríningu sa nepreukázalo byť výhodné.
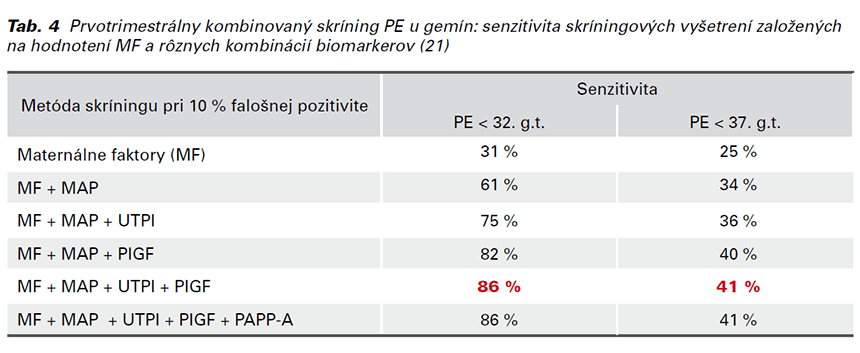
Prvotrimestrálny kombinovaný skríning jednoplodových gravidít, ktorý hodnotí MF + MAP + UTPI + PlGF pri cut-off 1:70, zachytí 90 % PE pred 32. týždňom a 75 % pretermínovej PE pri 10 % FP. Ak by sa pri skríningu gemín chcela dosiahnuť rovnaká senzitivita a použiť rovnaká cut-off hodnota, podarilo by sa síce zachytiť všetky pretermínové PE, ale pri 94 % FP. Takýto model by nespĺňal základné kritéria kvalitného skríningu. Preto FMF tím navrhuje zníženie cut-off hodnoty na 1:15, čím sa dosiahne nižšia FP (40 %) pri rovnakej senzitivite skríningu (75 %) pretermínovej PE. Okrem toho u gemín chýbajú jasné dôkazy o efektivite ASA ako prevencii PE, na čo sa plánuje prof. Nicolaides zamerať v novej rozsiahlej randomizovanej štúdii (21,22).
V súčasnosti obsahom mnohých odborných štúdií je včasná predikcia a prevencia PE. Jednoduchý skórovací systém predstavuje značnú nevýhodu vo vysokej FP a nízkej senzitivite oproti metóde kombinovaného skríningu, ktorý využíva prísne individualizovaný prístup ku každej pacientke. FMF tím vypracoval efektívny algoritmus pre výpočet rizika PE v 11. – 13.+6 gestačnom týždni, pri ktorom využíva hodnotenie MF, MAP, UTPI, PAPP-A a PlGF. V minuloročnej publikácii sa uvádzajú premenlivé cut-off hodnoty pri rôznych kombináciách skríningových stratégií, aj so zameraním na PAPP-A vs. PlGF. PAPP- A, ktorý sa v praxi bežne odoberá pri skríningu aneuploidií, má porovnateľné využitie v manažmente kombinovaného skríningu PE, ak sa cut-off nastaví podľa požadovanej senzitivity pri prijateľnej FP.
Vysokorizikovým pacientkam sa odporúča liečba aspirínom 150 mg vo večerných hodinách od 12. do 36. týždňa. Táto liečba vedie k signifikantnému poklesu výskytu PE, predovšetkým včasnej a pretermínovej formy, čím sa súčasne znižuje novorodenecká a maternálna morbidita.
Tento rok FMF tím vypracoval prvotrimestrálny kombinovaný skríning PE gemín. Je zrejmé, že budú potrebné ešte ďalšie sledovania a štúdie, optimálne prospektívne, randomizované a zaslepené na presnú analýzu efektívnosti skríningu PE a na hodnotenie prevencie PE podaním aspirínu u gemín.