









 Rada pro výzkum, vývoj a inovace: Seznam recenzovaných neimpaktovaných časopisů vydávaných v ČR
Oficielní časopis České společnosti pro ultrazvuk v porodnictví a gynekologii.
Rada pro výzkum, vývoj a inovace: Seznam recenzovaných neimpaktovaných časopisů vydávaných v ČR
Oficielní časopis České společnosti pro ultrazvuk v porodnictví a gynekologii.

Během těhotenství a kojení se podobně jako u dalších esenciálních živin zvyšuje poptávka po cholinu. Zároveň se předpokládá, že cholin je důležitý pro neurologický vývoj plodu a novorozence. Cholin je esenciální součástí buněčných membrán. Je to ve vodě rozpustná látka nezbytná pro metabolizmus metylové skupiny, syntézu neurotransmiterů, strukturální integritu a signální funkce buněčných membrán. Jako prekurzor neurotransmiteru acetylcholinu může ovlivňovat kognitivní funkce a vývoj mozku. Přímý vztah mezi kognitivními funkcemi dítěte a hladinou cholinu u plodu v děloze byl prokázán ve studiích na zvířatech, ale není dostatečně prokázán u lidí.
U cholinu se předpokládá, že by mohl snižovat hladiny homocysteinu. Vzhledem k tomu, že hyperhomocysteinémie je dávána do souvislosti s rozvojem kardiovaskulárních onemocnění, mohl by tak cholin kardiovaskulárnímu systému prospívat. Všechny tyto informace vedou ke zvýšenému zájmu o získání dostatečné evidence o významu příjmu cholinu v potravě a jeho případnou suplementaci. Těhotenství, kde se rozhoduje nejen o vývoji CNS, v tom může hrát klíčovou roli.
Cholin je esenciální součástí buněčných membrán. Je to ve vodě rozpustná látka nezbytná pro metabolizmus metylové skupiny, syntézu neurotransmiterů, strukturální integritu a signální funkce buněčných membrán (1).
Cholin je prekurzorem neurotransmiteru acetylcholinu, který může ovlivňovat kognitivní funkce a vývoj mozku (2). Během těhotenství a kojení se podobně jako u dalších esenciálních živin zvyšuje poptávka po cholinu (1). Zároveň se předpokládá, že cholin je důležitý pro neurologický vývoj plodu a novorozence (2,3). Přímý vztah mezi kognitivními funkcemi u dětí a hladinou cholinu u plodu v děloze byl prokázán ve studiích na zvířatech (4), ale není dostatečně prokázán u lidí.
Cholin jako prekurzor betainu může zvyšovat remetylaci homocysteinu na methionin (2). Hyperhomocysteinémie je dávána do souvislosti s rozvojem kardiovaskulárních onemocnění. U cholinu se předpokládá, že by mohl hladiny homocysteinu snižovat a prospívat tak kardiovaskulárnímu systému.
Nepodařilo se prokázat pozitivní vliv podávání cholinu u případů pokročilých stádií Alzheimerovy choroby (5). Na druhou stranu se u myší podařilo prokázat pozitivní vliv na výskyt kognitivního deficitu podobného Alzheimerově demenci při dlouhodobém preventivním užívání cholinu (6).
Všechny tyto informace vedou ke zvýšenému zájmu o získání důkazů o významu příjmu cholinu v potravě a jeho případnou suplementaci. Těhotenství, kde se rozhoduje nejen o vývoji CNS, v tom může hrát klíčovou roli.
Cholin se do lidského těla dostává potravou nebo je syntetizován de novo biosyntézou z fosfatidylcholinu (FCH) v hepatocytech (7). Betain, derivát cholinu, je navíc hlavním zdrojem metylové skupiny v potravě (8). Cholin je prekurzor fosfatidylcholinu, důležité součásti buněčných membrán, žluče a lipoproteinů. Účastní se také myelinizace neuroaxonů, buněčného dělení a lipidového transportu (9). Cholin hraje důležitou roli v syntéze acetylcholinu, a tím ovlivňuje cholinergní neurotransmisi (10). Může také zlepšovat signalizační procesy, které modulují placentární angiogenezi (11). Protože metabolizmus cholinu ovlivňuje řadu biologických procesů, je možné, že jeho nedostatečný příjem má komplexní vliv na zdraví člověka (12). Ukázalo se, že nedostatek cholinu vede ke snížení plazmatických koncentrací cholinu a FCH, a to i v erytrocytech (13). Cholinová deprivace způsobuje snížené shromažďování a vylučování lipoproteinu s velmi nízkou hustotou (VLDL) z jater (14). Mnoho studií prokázalo negativní účinky sníženého příjmu cholinu na zdraví, mezi něž patří steatóza jater, nealkoholická steatóza jater (NAFLD), homocysteinémie, poškození svalů (15), zhoršení kognitivních funkcí a karcinogeneze.
Těhotenství a kojení jsou stavy, které vyžadují vyšší příjem cholinu kvůli zvýšenému buněčnému dělení a membránové syntéze. Pro průkaz předpokládaného vlivu na vývoj mozku plodu a snížení rizika defektů nervové trubice není zatím dostatek solidních dat (16).
Cholin je absorbován v horním tenkém střevě pomocí specifických transportérů enterocytů cestou usnadněné difúze (9). Ukázalo se, že proteinový transportér cholinu (Choline Transporter Like-Protein 1 - CTL1) se podílí hlavně na absorpci cholinu v tenkém střevě a jeho funkce závisí na gradientu koncentrace cholinu a na elektrickém membránovém potenciálu. Tento transportér však není tkáňově specifický a je také exprimován v mnoha dalších tkáních. Absorpce cholinu a jeho následný metabolizmus závisí na jeho biochemické struktuře. Formy rozpustné ve vodě jsou absorbovány odlišně než formy rozpustné v lipidech.
Fosfatidylcholin (FCH) je téměř úplně absorbován v tenkém střevě (90 %) a rychle se objevuje v erytrocytech a jako součást lipoproteinů. FCH je štěpen pankreatickými enzymy, jako je fosfolipáza. Produkty této reakce jsou lysofosfatidylcholin a volné mastné kyseliny, které jsou absorbovány slizničními buňkami a resekretovány v chylomikronech jako nově vytvořený FCH nebo triacylglyceroly. I když doplňky FCH zvyšují koncentraci volného cholinu v séru 8-12 h po podání, neovlivňují koncentraci FCH v séru (17).
V krvi je volný cholin přítomen v nevázané formě, zatímco esterifikované choliny, jako je FCH, fosfocholin (FChol), sfingomyelin (SGM), jsou složkami lipoproteinů. Průměrná koncentrace cholinu v lidském séru je asi 10 mikromolů (18).
Cholin, který se neabsorbuje, může být metabolizován mikrobioty na trimetylamin (TMA) (19,20) a dále oxidován v játrech na trime-thylamin-N-oxid (TMAO) monooxygenázou 3 obsahující avin. Recentní studie prokázaly silnou pozitivní korelaci mezi zvýšenými koncentracemi TMAO v plazmě a kardiovaskulárními příhodami, ale mechanizmus však nebyl popsán (21-23).
FCH vzniká de novo reakcí katalyzovanou enzymem fosfatidylethanolamin-N-metyltransferázou (PEMT), která je indukována estrogenem (24). Samice jsou obecně odolnější vůči cholinové deficienci díky vysokým hladinám estrogenu. Během těhotenství mají ženy vysoké koncentrace cholinu a FCH je syntetizován účinněji. Těhotné ženy jsou tedy přirozeně chráněny před cholinovou deficiencí a jsou méně závislé na různých zdrojích cholinu v potravě. Díky tomuto přizpůsobení je k dispozici vyšší koncentrace cholinu během těhotenství a kojení, což je nezbytné pro správný vývoj plodu (25). Zvýšená exprese PEMT u žen však nemusí být dostatečná pro potlačení dietetické cholinové deficience (26). Na myším modelu bylo prokázáno, že exprese PEMTu v placentě a fetálních játrech je nízká nebo chybí a většina mateřského cholinu je transportována k plodu přes placentu (27). Postmenopauzální ženy léčené estrogenem mají nižší potřebu cholinu (25) a naopak, u žen s nedostatkem estrogenu jsou požadavky na obsah cholinu v dietě vyšší. Muži jsou náchylnější k depleci cholinu, protože mají nízké hladiny estrogenu.
Metabolizmus cholinu úzce souvisí s metabolizmem folátu. Snížená dostupnost cholinu zvyšuje poptávku po folátové metylové skupině (28). Protože pro tento proces jsou zapotřebí metylové skupiny pocházející z kyseliny listové, vede nedostatek kyseliny listové ke zvýšení koncentrace FCH v séru, zatímco doplnění kyseliny listové vede ke zvýšené koncentraci FCH (29).
Prenatální faktory, včetně mateřské stravy, mohou ovlivnit vývoj plodu. Účinky prenatálních spouštěčů lze pozorovat brzy postnatálně, ale také později v životě. Tento proces se nazývá fetální programování a úzce souvisí se zapojením tzv. jednouhlíkového metabolizmu (30,31). Zdá se, že epigenetické mechanizmy, které regulují genovou expresi a tím ovlivňují fenotyp, mohou být spojením mezi perinatální výživou a metabolizmem v dospělosti (32). Bylo prokázáno, že mateřský příjem folátu a cholinu během těhotenství může vyvolat trvalé modifikace metylačních vzorců u plodu (33-36). Výsledky však nejsou jednoznačné, protože jiné studie vliv na metylaci DNA na deficienci folátu během prenatálního života neprokázaly (37). Byl také testován programovací potenciál celkových dietních omezení. Mohou sice změnit jednouhlíkový metabolizmus březích samic, ale nevedou k trvalým metabolickým změnám pozorovatelným u jejich gravidního potomstva (38). Nedostatek potravy během těhotenství může indukovat změny v expresi genů zapojených do modifikace histonů a metylace DNA (39).
Cholin je pozitivně nabitá molekula, a proto je zapotřebí, aby byl lipidovou membránou přenášen proteinovým mechanizmem. Na transportu cholinu přes buněčné membrány se podílejí různé typy proteinů. Byly použity kinetické metody k prokázání dvou typů transportu cholinu: prvním je usnadněná difúze v erytrocytech (40) a přes hematoencefalickou bariéru, druhým aktivní transport v jiných tkáních. Vysoce účinné cholinové transportéry, které jsou závislé na Na+ a Cl-, jsou základními faktory signalizační funkce acetylcholinu v centrálním a periferním nervovém systému. Cholinergní systém reguluje mnoho kognitivních funkcí, jako je paměť, pozornost a procesy učení, ale také reguluje funkce fyziologické jako například kontrakce hladkých a kosterních svalů a modulaci srdeční frekvence (41,42). Syntéza acetylcholinu se vyskytuje ve všech cholinergních neuronech a probíhá přenosem cholinu přes cholinové transportní mechanizmy (CHT) (43). U myší vede genotyp Cht -/- k nehybnosti, nepravidelnému dechu a smrti do hodiny po narození. Na druhé straně, myši Cht +/-, které přežily navzdory nižším množstvím transportérů, byly životaschopné a plodné. Je zajímavé, že vychytávání cholinu u těchto myší bylo na stejné úrovni jako u myší divokého typu (44). Lidský CHT má 5 alelických variant, které jsou spojeny s presynaptickým vrozeným myastenickým syndromem (45). Pacienti s touto poruchou jsou snadno unavitelní a trpí slabostí svalů končetin, očí, obličejových a bulbárních svalů (46). Výskyt této choroby je jeden až dva lidé na 500 000 (47). Ve stejném genu CHT vede další delece (1-BP DEL, 1497G) k autozomálně dominantní distální hereditární motorické neuropatii typu VIIA, což je nejčastěji dědičná porucha periferního systému a postihuje jednu osobu z 2 500 (48). Mezi klinické příznaky tohoto onemocnění patří ztráta distálních svalů a slabost (49). Všechny tyto příklady naznačují důležitou roli, kterou hraje transportér CHT ve vývoji nervového systému.
Protože plod má omezenou schopnost syntetizovat fosfatidylcholin v játrech, je závislý na přísunu cholinu od matky přes placentu (50). Aktivní transport mezi mateřským a plodovým oběhem zajišťují přenašeče cholinu. Cholinové transportéry v placentě nejsou příliš probádané a není zcela jasné, které transportéry se na přísunu cholinu podílejí.
Role folátových a cholinových transportérů ve vývoji plodu se stále studuje. Alelické varianty genů pro PCFT (protonový folatátový transportér) a CHT mohou vést k závažným onemocněním. Pro hlodavce může být narušení genů Rfc, Fra a Cht smrtelné. Tyto výsledky naznačují, že role uvedených transportérů je relevantní pro vývoj plodu. Nepodařilo se zatím prokázat souvislost mezi geny kódujícími tyto proteiny a perinatálními výsledky. Počet studií, které měly analyzovat transportéry cholinu a folátu ve vztahu k vývoji plodu, je velmi omezený a příliš malý na to, aby bylo možné správně posoudit roli těchto transportérů na vývoj plodu a bez dalších studií nelze činit závěry o vlivu transportních genů na stav folátů a cholinu.
Bylo prokázáno, že mateřské hladiny cholinu a folátu během těhotenství ovlivňují vývoj plodu (1,2). Doporučená denní dávka (RDA - recommended daily allowance) pro příjem folátu v těhotenství je 600 μg ekvivalentů folátu (51). Navíc se před a během těhotenství doporučuje suplementace kyselinou listovou. V několika zemích, včetně USA a Kanady, je přidávání kyseliny listové do potravin, jako jsou chléb, těstoviny nebo cereálie, povinné. (51). Požadavky na suplementaci cholinem nebyly akceptovány (21,52), ale v roce 1998 Rada pro výživu Národní akademie věd USA cholin uznala poprvé za nezbytnou součást stravy. Současně stanovila doporučení pro přiměřený příjem cholinu: 7,5 mg na kg tělesné hmotnosti na den. Pro netěhotné bez udání váhy 425 mg/den, pro těhotné 450 mg/den. Pro zajímavost, pro muže stanovila dávku 550 mg/den.
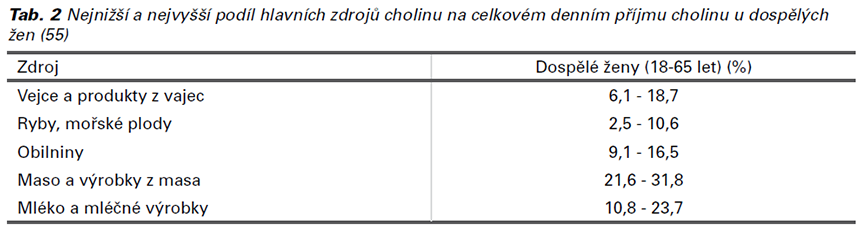
Pro těhotné a kojící ženy byl doporučen vyšší příjem cholinu, aby byl zaručen jeho dostatečný přísun vyvíjejícímu se plodu. Ministerstvo zemědělství USA analyzovalo obsah cholinu ve stovkách potravinových produktů a vytvořilo databázi obsahu cholinu v běžných potravinách (53). Nejbohatšími zdroji cholinu jsou vejce, maso a celozrnné obilniny (54).

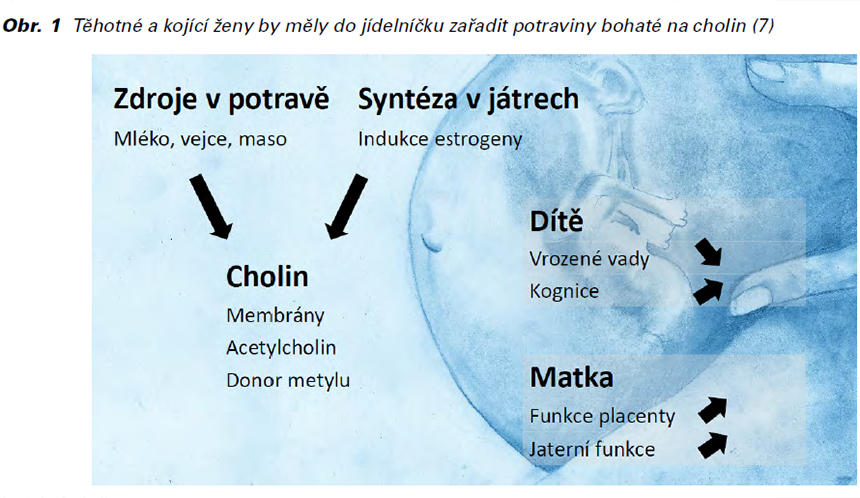
Přísun živin k plodu je zásadní pro jeho správný vývoj. Závisí na nutričním stavu matky a přenosu živin od matky k plodu. Během prenatálního vývoje jsou požadavky na přísun cholinu vysoké: plod roste, placenta se zvětšuje, dochází ke zvýšené metylaci DNA a dalším fyziologickým procesům (1,2,51). Dostatečné hladiny cholinu jsou zvláště důležité pro vyvíjející se mozek: je prekurzorem acetylcholinu, klíčového neurotransmiteru pro regulaci proliferace neuronů, diferenciaci, migraci, zrání, plasticitu a přežití, ale také pro tvorbu synapsí (3,21,52-54). Cholin také poskytuje substrát pro tvorbu fosfatidylcholinu a sfingomyelinu, hlavní složky neuronálních a dalších buněčných membrán potřebných pro přenos signálů, vývoj mozku a růst plodu (4,6,56).
Výsledky některých studií (9,22,26) uvádějí vliv cholinu na hladinu lipidů a kardiovaskulární systém. Jedná se však o výsledky nekonzistentní, s nízkou výpovědní hodnotou a bez kvalitních prospektivních randomizovaných studií. Observační studie naznačují, že cholin může být prospěšný pro neurologické zdraví, zejména pro kognitivní funkce, a pro citlivost na inzulín. Cholin musí být dostupný během kritického období vývoje plodu a dítěte. Pokud tomu tak není, geny, které řídí vývoj mozku a funkci placenty, jsou chybně naprogramovány a může být narušena jejich funkce. To může vést k abnormálnímu vývoji mozku, abnormální funkci placenty a preeklampsii (57).

Publikace byla podpořena výzkumným záměrem RVO-VFN64165.